Chromatographie von Blattfarbstoffen
Allgemeine Hinweise zum Experimentieren und Disclaimer beachten!
Einleitung
Im Herbst verfärben sich die Blätter sämtlicher Bäume und werden bunt. Doch wie kommt es eigentlich dazu? Um eine Erklärung zu finden, müssen die Blätter zuerst mit geeigneten Verfahren untersucht werden. Hierbei ist die Auftrennung via Dünnschichtchromatographie und UV/VIS-Spektroskopie am zweckmäßigsten.
Schwierigkeitsgrad
Schülerexperiment, mittel
Geräte
Macherey-Nagel DC Platten ALUGRAM Sil G/UV254 5x7,5 cm, Mikroliterpipette 1-5 µl mit passenden Spitzen, Schraubdeckelglas, Reibschale mit Pistill, Quarzsand, Faltenfilter, Pasteurpipette, Reagenzglas und Reagenzglasständer, Messpipetten, Bleistift und Geodreieck, Pinzette, UV/VIS-Spektrometer, PS Küvetten
Chemikalien
Ethanol
Ethylacetat
Cyclohexan
Hinweis
DC Platten niemals ohne Handschuhe angreifen, da Feuchtigkeit die Trennleistung mindert. Kurzwelliges UV-Licht ist für die Augen sehr schädlich!
Durchführung
Vorbereitung:
Zuerst wird das Probenmaterial besorgt: Das können z.B. Blätter von Bäumen sein. Stehen diese nicht zur Verfügung, eignet sich auch eingefrorener Spinat hervorragend für dieses Experiment.
Das pflanzliche Material wird dann im Mörser mit etwas Sand versehen und vollständig mit Ethanol bedeckt. Durch Zerreiben werden die Pflanzenfarbstoffe rasch extrahiert und der Ethanol nimmt eine intensiv-grüne Farbe an. Durch Filtration über einen Faltenfilter werden alle störenden Schwebstoffe entfernt. Insbesondere für die UV/VIS-Spektroskopie muss die Probenlösung klar sein.
Dünnschichtchromatographie:
Für die Dünnschichtchromatographie muss zuerst das Laufmittel hergestellt werden: Dazu wird Cyclohexan und Ethylacetat im Verhältnis 3:1 gemischt. Für ein handelsübliches 450 g Marmeladenglas – das als Entwicklungskammer zweckentfremdet wird - sind ca. 10-15 mL Laufmittel notwendig. Es werden also zuerst 9 mL Cyclohexan gefolgt von 3 mL Ethylacetat in das Glas pipettiert und durch Schwenken vermischt. Um die Kammer mit Dampf zu sättigen, werden die Wände mit Küchenpapier ausgekleidet. Durch den Kontakt mit dem Laufmittel haften diese von selbst am Glas.
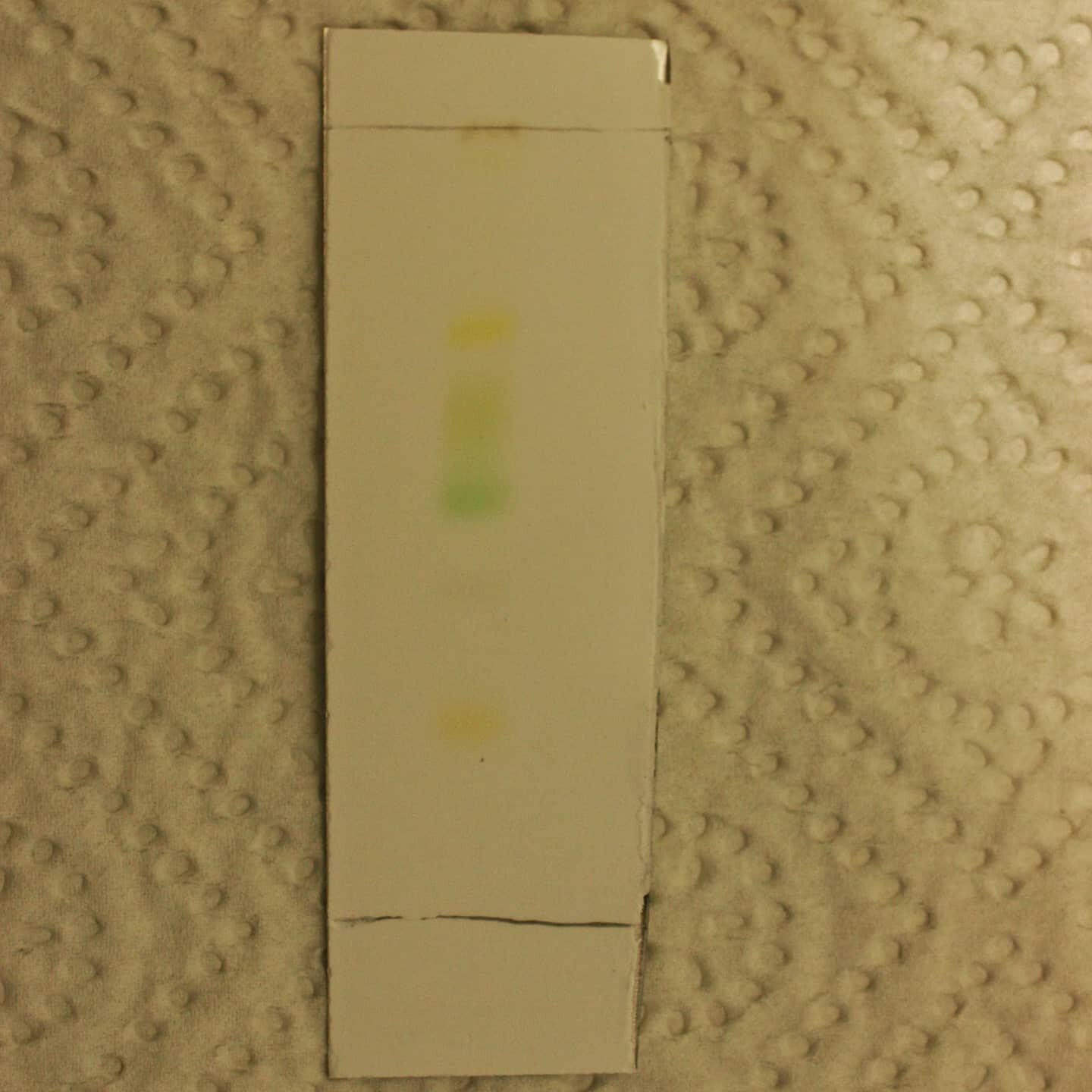
Während sich die Kammer äquilibriert, wird die DC Platte vorbereitet. Dazu wird 1 cm über dem unteren Rand der DC Platte unter Zuhilfenahme eines Geodreiecks ein gerader Strich mit einem weichen Bleistift gezeichnet. Auf dieser Hilfslinie werden dann mittels Mikroliterpipette 3x 5 µl Blattextrakt aufgetragen. Zwischen den Intervallen muss die Platte kurz trocknen, ansonsten breiten sich die Substanzflecken zu weit aus. Das Ziel ist, Substanzflecken in der Größe von 2-3 mm zu haben, um eine optimale Trennung zu gewährleisten. Es funktioniert sehr gut, mehrere Substanzflecken aneinander zu setzen, so dass die Auftragungszone entlang der Hilfslinie größer wird. Die Kieselgel-Schicht darf während des Auftragens nicht beschädigt werden.
Die betüpfelte DC Platte wird aufrecht in die Entwicklungskammer gestellt. Durch Kapillarkräfte steigt das Laufmittel entlang der Platte nach oben. Ist die Laufmittelfront nach 5-10 min ca. 1 cm vom oberen Rand entfernt, wird die DC-Platte mit einer Pinzette aus der Kammer genommen und die Laufmittelfront eingezeichnet, um später den Rf-Wert zu berechnen.
Die luftgetrocknete DC-Platte kann nun unter kurzwelligem (254 nm) und langwelligem (366 nm) UV-Licht betrachtet werden. Auf der DC-Platte befindet sich ein Fluoreszenzindikator, der unter kurzwelligem UV-Licht grün fluoresziert. Durch Fluoreszenzlöschung erscheinen Substanzflecken dunkel. Unter langwelligem UV-Licht besitzen manche Farbstoffe selbst eine Fluoreszenz. Auch die Betrachtung unter sichtbarem Licht eignet sich bei farbigen Substanzen.
Der Rf-Wert wird nach folgender Formel berechnet:
Rf = Laufstrecke Substanz / Abstand Auftragunglinie zur Laufmittelfront
UV/VIS-Spektroskopie:
Die Probenlösung wird mit einer Pasteurpipette in eine Küvette aus Polystyrol überführt und im UV/VIS-Spektrometer gemessen.
Entsorgung
Alle Lösungsmittel kommen in den Behälter für organische, halogenfreie Abfälle.
Erklärung
Dünnschichtchromatographie:
Die mobile Phase – das Laufmittel - schleppt alle Farbstoffe mit. Diese haben aber aufgrund ihres unterschiedlichen Aufbaus unterschiedlich starke Wechselwirkungen mit der stationären Phase – dem Kieselgel. Manche Farbstoffe werden vom Kieselgel stärker zurückgehalten, andere schwächer. Das führt zu einem Trenneffekt und das zuvor homogene Gemisch kann in seien Bestandteile zerlegt und analysiert werden.
UV/VIS-Spektroskopie:
Im UV/VIS-Spektrometer wird Licht mit definierter Wellenlänge auf die Probe gestrahlt und mit einem Detektor gemessen, wie viel davon absorbiert wird. So absorbieren Chlorophyll A und B blaues und rotes Licht, reflektieren aber grünes Licht (weshalb wir Pflanzen als „grün“ wahrnehmen). Aber wie die Dünnschichtchromatographie gezeigt hat, besteht der Blattextrakt nicht nur aus grünem Chlorophyll – auch im UV/VIS-Spektrum kann das Absorbtionsmaximum von beta-Carotin bei 475 nm identifiziert werden.
Antwort auf die Eingangsfrage: Warum verfärben sich die Blätter im Herbst ?
Würde man ein Blatt aus dem Sommer und eines aus dem Herbst vergleichen, würde man sehen, dass die Rf-Werte gleichbleiben – also dieselben Substanzen im Blatt vorkommen. Was sich ändert, ist die Zusammensetzung. Grünes Chlorophyll wird im Herbst tiefer im Stamm eingelagert, orange und rote Carotinoide bzw. Xantophylle kommen dann zum Vorschein.